Hipoplasia Cartilagem Cabelo
A Hipoplasia Cartilagem Cabelo (HCC) é uma displasia óssea que apresenta baixa estatura, cabelo fino e em pouca abundância, variados graus de imunodeficiência, anemia e problemas gastrointestinais.
É também conhecida por síndrome de McKusick pois foi identificada pelo geneticista americano Victor Almon McKusick, pioneiro no mapeamento do genoma humano e na genética médica.
O que é a HCC1,2?
Trata-se de uma condição hereditária rara com padrão de hereditariedade autossómico recessivo. Tem a sua maior prevalência na população finlandesa (cerca de 1 em cada 23 000 nascimentos1) e nos Old Order Amish2 . As comunidades Amish consistem em grupos de pessoas fundados por um pequeno número de casais, com ascendência partilhada, que permanecem isoladas do resto da sociedade e são propensas a padrões recessivos de hereditariedade.
 Fig. 1. McKusick documentou tudo com a sua máquina fotográfica. Créditos: Aquivo Johns Hopkins
Fig. 1. McKusick documentou tudo com a sua máquina fotográfica. Créditos: Aquivo Johns Hopkins
Um pouco de história
Um artigo publicado na década de 50 que identificou altas taxas de acondroplasia nas comunidades Amish da Pensilvânia despertou a curiosidade de McKusick. Isto porque, a acondroplasia é uma condição autossómica dominante, portanto, pouco provável de ser mais prevalecente nos Amish do que na população geral.
McKusick dedicou-se, então, a estudar famílias com alterações hereditárias nestas comunidades e descobriu dois tipos diferentes de condições raras recessivas: a HCC e a síndrome de Ellis-van Creveld (as pessoas apresentam 6 dedos). Depois destas descobertas, McKusick passou décadas a estudar a genética dos Amish, investigando registos genealógicos e hospitalares, visitando famílias para examinar fenótipos, documentar sintomas e recolher amostras.
O trabalho de McKusick levou a uma maior compreensão das características e dos factores de risco associados a muitas condições hereditárias e contribuiu para o seu livro Mendelian Inheritance in Man (MIM), um catálogo abrangente de genes humanos e doenças hereditárias. Hoje, este catálogo persiste como uma base de dados online, OMIM, e contém informação sobre mais de 15.000 genes.
O que causa a HCC1,3?
A HCC é causada por mutações no gene RMRP. Cada um dos progenitores de um bebé com HCC tem uma cópia do gene mutado, contudo não apresentam sinais ou sintomas. Isto acontece porque a HCC é uma condição autossómica recessiva, o que significa que a pessoa com HCC recebeu duas cópias do gene com a mutação, uma de cada progenitor. Uma pessoa com apenas uma cópia desta mutação não será afetada, mas transportará o gene com mutação.
A HCC é uma condição muito rara pois a probabilidade de encontrar outra pessoa com a mutação no gene RMRP é extremamente baixa. Esta probabilidade aumentará se duas pessoas partilharem laços consanguíneos. O diagnóstico e aconselhamento genético são importantes se esta última situação se verificar.
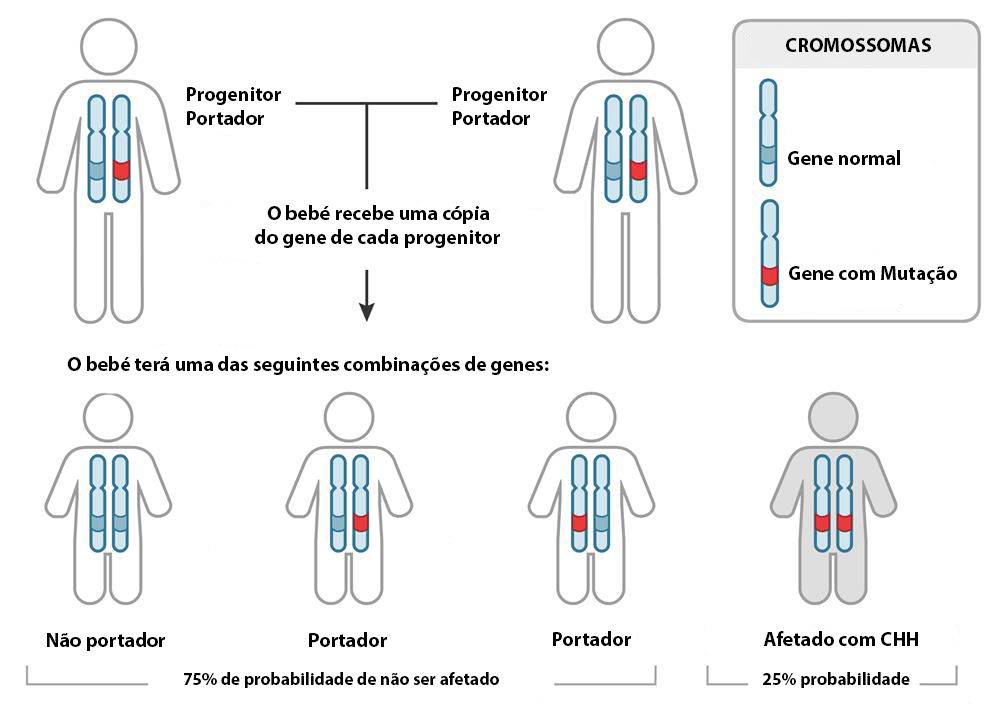
Fig. 2. Hereditariedade autossómica recessiva
Características Clínicas e Radiológicas4,5,6,7
-
Baixa estatura
-
Ossos longos (braços e pernas) crescem mais devagar
-
Malformações nas metáfises
-
Genu varum
-
Hipermobilidade articulatória: ligamentos das mãos, pulsos e pés muito flexíveis
-
Limitação na articulação do cotovelo
-
Lordose e escoliose
-
Cabelo, pestanas e sobrancelhas em pouca ambundância (hipotricose), finos e claros
-
Sistema imunitário comprometido, de forma variável: pessoas com problemas mais graves (SCID) são muito susceptíveis a infecções persistentes e recorrentes. A varicela pode causar graves infecções nas pessoas com HCC. As crianças devem ser avaliadas por um imunologista antes das vacinas habituais, nomeadamente a da varicela.
-
Problemas gastrointestinais: absorção deficitária de nutrientes ou intolerância ao glúten; doença de Hirschsprung, uma doença gastrointestinal que provoca obstipação intestinal e inchaço do cólon
-
Maior risco de desenvolver cancro, particularmente carcinomas (cancro da pele), leucemia (medula óssea) e linfomas7.
 |
|
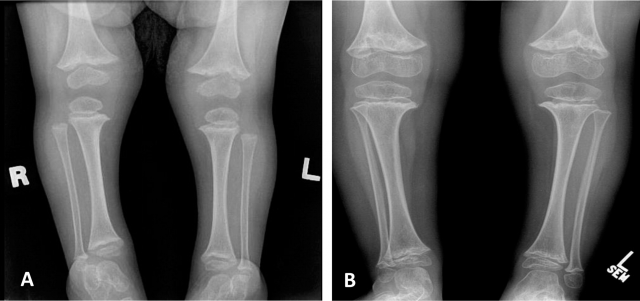
Fig.3. Radiografia das extremidades inferiores de criança com 2 (A) e 4 (B) anos de idade mostram alterações metafisárias típicas e lucências císticas irregulares de margens escleróticas e aparência fragmentada. |
|
Fig.4. Radiografia das mãos aos 4 anos demonstra típico encurtamento dos metacarpos e alterações metafisárias (distal radial e ulnar). |
 |
|
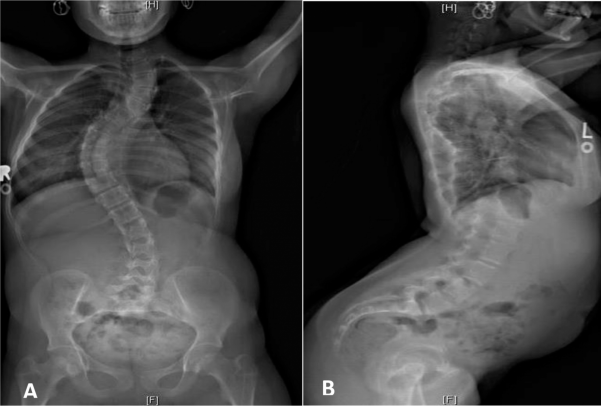
Fig.5. Vistas posterior e lateral da coluna vertebral aos 13 anos, mostram escoliose toracolombar multisegmentária com levoscoliose torácica superior, dextroscoliose torácica inferior e levoscoliose lombar. Fonte: Lymphosign.com |
Diagnóstico2,3
O diagnóstico é alcançado através de avaliação clínica e da identificação de características radiológicas e análises genéticas. Para além das mutações no gene RMRP é possível que o diagnóstico de HCC possa ser sinalizado pelas epífises em forma de cone nas falanges das mãos.
As crianças diagnosticadas com HCC devem fazer uma avaliação imunológica completa para determinar a presença de imunodeficiência. É possível fazer um diagnóstico intrauterino através de recolha e análise de líquido amniótico (amniocentese) e da biópsia de vilosidades coriónicas (CVS). Métodos utilizados no caso de haver maior suspeita, por exemplo, se houver um irmão com a mesma condição.
A HCC também pode ser diagnosticada antes do nascimento através de um exame ecográfico para verificar o encurtamento e abaulamento do fémur, observável, por vezes, na ecografia.
Tratamento2
Não há ainda qualquer terapêutica que cure, previna ou reverta a HCC. Os objetivos de tratamento passam por apoiar o desenvolvimento físico e social, prevenir e tratar quaisquer complicações de saúde que surjam.
O alongamento ósseo é uma possibilidade e pode significar uma maior funcionalidade no dia a dia e mais autonomia. A elegibilidade para este tipo de tratamento depende de vários fatores, como idade, altura e os problemas funcionais daí resultantes. Os benefícios e adversidades deste procedimento devem ser abertamente discutidos, pois o risco de complicações, dor associada, duração do processo e motivação da criança para o fazer são fatores importantes.
É fundamental que a pessoa com HCC seja acompanhada por uma equipa médica multidisciplinar para acompanhar a função imunitária. Contudo, é sempre importante consultar um médico caso haja febre que dure mais do que uma semana, perda de peso sem explicação aparente ou nódulos linfáticos.
Investigação
As tentativas de criar um modelo animal de HCC que permita testar terapias ainda não tiveram sucesso. A investigação poderá levar anos para desvendar o mecanismo patogénico desta condição e encontrar um tratamento, tal como na acondroplasia, onde passaram mais de 20 anos entre a identificação do gene responsável e as soluções terapêuticas eficazes.
O Desafio Social
O dia a dia na escola e a vida social podem ser um desafio para crianças e jovens com características físicas diferentes. Discutir com a equipa escolar as questões relacionadas com a inclusão e diferença física é importante e, se necessário, os pais devem procurar aconselhamento psicológico para a criança ou jovem.
Este é um aspeto crucial. Em conjunto com o acompanhamento clínico prestado pelo médico, pais, criança e escola formam uma equipa com um projeto comum que consiste em apoiar social e emocionalmente a criança e promover a sua autonomia, desenvolvimento e resiliência.
Bibliografia
- 1. Mäkitie O. Cartilage-hair hypoplasia in Finland: epidemiological and genetic aspects of 107 patients. J Med Genet. 1992 Sep;29(9):652-5.
- 2. Ridanpää M, Jain P, McKusick VA, Francomano CA, Kaitila I. The major mutation in the RMRP gene causing CHH among the Amish is the same as that found in most Finnish cases. Am J Med Genet C Sem Med Genet. 2003 Aug 15;121C(1):81-3
- 3. Bonafé, L., et al. (2002). RMRP gene sequence analysis confirms a cartilage-hair hypoplasia variant with only skeletal manifestations and reveals a high density of single-nucleotide polymorphisms. Clinical Genetics, 2(61), 146-51
- 4. Riley P Jr, et al. Cartilage hair hypoplasia: characteristics and orthopaedic manifestations. J Child Orthop. 2015 Apr;9(2):145-52. doi: 10.1007/s11832-015-0646-z. Epub 2015 Mar 13. PMID: 25764362; PMCID: PMC4417732
- 5. Mäkitie O, Kaitila I. Cartilage-hair hypoplasia--clinical manifestations in 108 Finnish patients. Eur J Pediatr. 1993 Mar;152(3):211-7. doi: 10.1007/BF01956147. PMID: 8444246
- 6. Ashby GH, Evans DI. Cartilage hair hypoplasia with thrombocytopenic purpura, autoimmune haemolytic anaemia and cell-mediated immunodeficiency. J R Soc Med. 1986 Feb;79(2):113-4. doi: 10.1177/014107688607900216. PMID: 3950893; PMCID: PMC1290197
- 7. Mäkitie O, Pukkala E, Teppo L, Kaitila I. Increased incidence of cancer in patients with cartilage-hair hypoplasia. J Pediatr. 1999 Mar;134(3):315-8. doi: 10.1016/s0022-3476(99)70456-7. PMID: 10064668
A ANDO agradece à Claudia Sousa e à sua família, associados da ANDO. Em especial ao seu filho Francisco, que aparece na foto de rosto desta página.
Saiba mais sobre:
-
O processo de inovação e desenvolvimento (I&D) de medicamentos para doenças raras
-
A Dor nas displasias ósseas aqui

